Bonjour, j’aimerais clarifier quelques petits trucs..
Si on a cette représentation de BF3 :
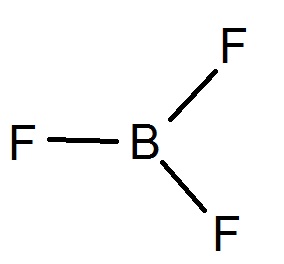
Je me demande comment on fait pour savoir si le B porte un doublet non liant ou pas (peut être qu’il est pas représenté) (ou plusieurs). Je pense avoir trouvé cette technique mais pourriez vous me dire si j’ai la bonne méthode et si mes bases sont justes ?
Pour B, Z=5 donc
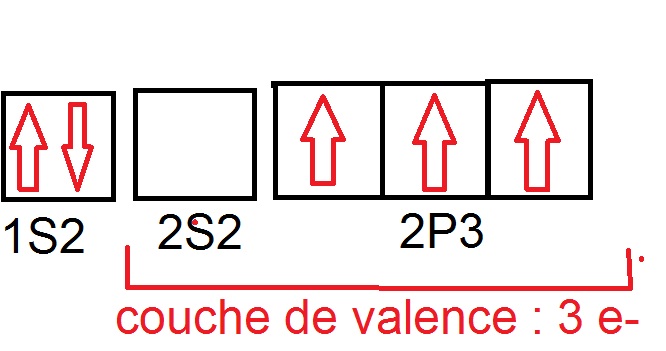
3 électrons sont impliqués dans les liaisons, on en a 3 de valence, il n’y en a pas qui reste et qui pourrait former un doublet non liant.
Alors, qu’en pensez vous ?
Merci
Comment as-tu rempli tes cases quantiques ??
La configuration électronique du bore est : 1s2 2s2 2p1
Donc 2 électrons dans la case 1s , 2 dans la 2s et 1 seul dans les 3 cases 2p.
Ce qui ne change rien au nombre d’électrons de valence, le bore en a 3, donc si il fait 3 liaisons, il n’aura pas de doublets non liants mais une lacune électronique.
Ha oui c’est quand on a des ions qu’on doit « retirer d’abord les e- de la s »  là il n’y a rien à retirer du tout !
là il n’y a rien à retirer du tout !
On a donc :
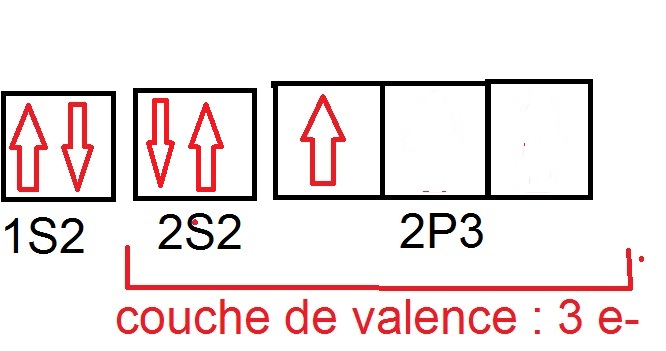
Mais du coup ça fait deux électrons appariés sur la couche de valence et un e- tout seul, mais deux électrons appariés ça fait un doublet non ? Du coup on a à placer sur la représentation 1 doublet, et 1 e- seul !? je comprends plus rien..
L’atome de Bore possède simultanément des doublets électroniques et des orbitales vides accessibles sur sa couche de valence, son excitation peut conduire à une augmentation de la valence, appelée promotion de valence interne :

La couche de valence du Bore est alors constituée de 3 électrons célibataires pouvant former des liaisons, et d’une orbitale vacante représentée par un rectangle vide et appelée lacune électronique.
Le schéma de Lewis de BH3 met en évidence 3 liaisons simples B – H. Il y a, dans ce cas, 6 électrons de valence autour de l’atome de bore qui ne respecte donc pas la règle de l’octet. Ces entités dans lesquelles un atome est déficitaire d’au moins une paire électronique pour satisfaire la règle de l’octet présentent une tendance naturelle à pallier cette insuffisance : ce sont des acides de Lewis, c’est-à-dire des accepteurs de doublets.

En pratique, quand on écrit la formule de Lewis de BH3, on sait qu’on doit placer 6 électrons de valence (1 par Hydrogène et 3 pour le Bore) soit 3 doublets qui correspondent aux 3 liaisons B-H (doublets liants). Il n’y a donc pas de doublet non liant sur le Bore, mais une lacune électronique indiquant que celui-ci est déficitaire en électrons.
Ok j’ai très bien compris 
J’en profite pour te poser une autre question ? y a t il un moyen plus simple que de remplir des cases quantiques (ça peut être long) pour savoir le nombre d’électrons de valence d’un atome isolé ?
merci 
De rien 
Une solution est d’utiliser le nombre d’électrons par période (n=1,2,3…) :
**- 1ère période : 2 e-
- 2ème et 3ème période : 8 e-
- 4ème et 5ème période : 18 e-**
Exemple : silicium Si Z=14
14 = 2 (1ère période) + 8 (2ème période) + 4 (3ème période)
La 1ère et la 2ème période sont remplies (électrons de coeur) et la 3ème période est incomplète (électrons de valence). Le silicium possède donc 4 électrons de valence, sa structure externe est : 3s23p2
On peut écrire sa configuration électronique en fonction de celle du gaz rare qui le précède dans la classification : le néon (périodes 1 et 2 remplies donc Z = 2 + 8 = 10) : [Si] = [Ne]3s23p2 (couche de valence en rouge)
A partir de la 4ème période, il faut tenir compte des orbitales d.
Exemple : arsenic As Z=33
33 = 2 (1ère période) + 8 (2ème période) + 8 (3ème période) + 15 (4ème période)
La 4ème période est incomplète et comporte 15 électrons, donc 10 électrons appartenant à la couche 3d qui est donc complète et ne fait partie de la couche de valence. L’arsenic possède donc 5 électrons de valence, sa structure externe est : 4s24p3
Le gaz rare qui le précède est l’argon (période 3 donc Z = 2 + 8 + 8 = 18) donc : [As] = [Ar]3d104s24p3 (couche de valence en rouge)
Merci pour ta réponse très développée et claire.
Donc en fait, plutot que de faire des cases quantiques tu fais des formules comme 4s24p3 c’est ça ? Et donc la couche de valence c’est que les derniers numéros identiques c’est ça ?
Mais si par exemple j’ai 4s23d5, la couche de valence c’est laquelle ? les e- de valence ?
Oui, la configuration électronique peut s’écrire en mettant le type de l’orbitale (1s, 2s, 2p…) suivi du nombre d’électrons (en exposant).
Les électrons de valence correspondent aux électrons des couches de nombre quantique principal n le plus élevé et à ceux des sous-couches (n-1)d et (n-2)f non saturées.
Donc dans ton exemple, 4s23d5 est la couche de valence car la couche 3d est partiellement remplie. Il y a donc 7 électrons de valence.




