bonjour on me demande la représentation de lewis de l’acide sulfurique (H2SO4)
moi j’ai fait celle ci:
[attachment=0]Sans titre.JPG[/attachment]
et sur google je trouve celle la:
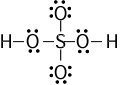
j’aimerai savoir si les deux sont justes.de plus doit on représenter les doublets non liants par 2 points ou un tiret?
merci d’avance
Seule la seconde est acceptable. Pour bien le voir, on peut penser aux degrés d’oxydation de l’oxygène : tous les oxygènes présents doivent être au degré d’oxydation -2.
Ta représentation de lewis n’est pas fausse, mais la « bonne » formule est celle de wikipedia, c’est juste une question de culture chimique. En fait c’est surtout a cause de tes liaisons peroxo…ca serais connu si l’acide sulfurique avait des proprietées radicalaire…
Au risque de jouer les trouble-fête: les deux formules sont complètement fausses
…O
…||
H-O-S-O-H
…||
… O
Enfin chaque O possède deux doublets (en plus) [il faut mettre des tirets] et il ne faut pas les oublier en représentation de Lewis. Sur la formule de google, les oxygène sont chargés!!!
Bonne semaine.
un S avec 6 liaisons? gné???

Celle-ci est la plus probable. En effet, le nombre d’oxydation de l’oxygène est de -II, et les atomes ne sont pas chargés.
Et oui, le soufre peut former 6 liaisons covalentes.
Le soufre est dans la 3e ligne de la CP, il peut donc être hypervalent.
Par contre pour la représentation des doublets non liants, les deux sont permis je crois : mon prof de spé mettait (et met toujours !!) deux petits points côte à côte, mais pas de tiret.
mais le fait que le souffre et l’oxygene soit sur la meme colonne, ca ne veut pas dire qu’ils ont le meme nombre d’electrons libres? et donc le meme nombre de liasons?
Oui et non : ils ont le même type de structure électronique, mais le soufre peut être hypervalent car les niveaux d’énergie supérieurs sont accessibles plus facilement.

